 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列鰲合物的磁矩,画出它们中心离子的价层电子分布,并指出其空间构型.这些螯合物中哪种是
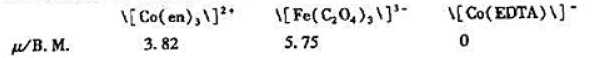
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
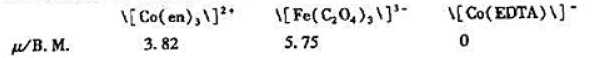
 答案
答案
 更多“已知下列鰲合物的磁矩,画出它们中心离子的价层电子分布,并指出其空间构型.这些螯合物中哪种是”相关的问题
更多“已知下列鰲合物的磁矩,画出它们中心离子的价层电子分布,并指出其空间构型.这些螯合物中哪种是”相关的问题
第1题
和t2g轨道中的分布,并估计它们的磁矩各约为多少(B.M.).指出这些配合物中何者为商自旋排布,何者为低自旋排布.
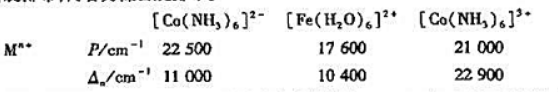
第3题
(1)/[CuCl2/]-(直线形);
(2)/[Zn(NH3)4/]2+(四面体形);
(3)/[Co(NCS)4/]2-(四面体形).
第6题
第7题
研究发现棕色配位化合物[Fe(NO)(H2O5)]SO4显顺磁性,并测得其磁矩为 3.8μa。
(1)试给出中心离子d电子的排布方式及杂化轨道类型;
(2)[Fe(NO)(H2O5)]SO4中N—O键的键长与自由NO分子中键长相比,
变长还是变短?试简述理由
第9题
命名下列配合物并指出中心离子、配体、配位原子、配位数、配离子电荷.
[CoCl3(NH3)3] 、K2[Ni(CN)4]、Na3[SiF6]、K3[Fe(SCN)6]
第10题
已知电子沿着团环运动(如图C.3.1)的势能函数V为:
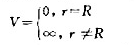
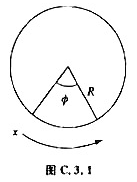
r是电子到四环中心的距离。其Schrodinger方程为:
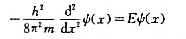
将变数x改成与角度有关的函数,x=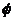 R,解此方程可得波函数
R,解此方程可得波函数
ψn和相应能量En的表达式如下:

(1)以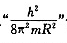 作能量单位,作图示出能级的高低及能简并情况。
作能量单位,作图示出能级的高低及能简并情况。
(2)画出吡啶(C5H5N)和吡咯(C4H4NH)的价键结构式。将环中的π电子运动情况近似地看作如图C.3.1所示的状态,说明环中π键电子的数目,以及它们的LUMO和HOMO。将电子从HOMO跃迁到LUMO,哪一种化合物所需的光的波长短些?
(3)在吡啶盐酸盐(C5H5NH+•Cl-)中。正离子中π键电子数是多少?为什么中性的吡咯C4H4NH能稳定存在,而中性的C5H5NH不稳定?
(4)联系讨论单环共轭多烯体系4m+2规则的本质。