 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某反应:A(g)+B(s)=C(g)+D(s)的ΔrH=-80.25kJ。反应在300K,100kPa下发生,体系做了最大功
并放热4.86kJ.试求反应过程的Q、W、ΔrU、ΔrS和ΔrG。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
并放热4.86kJ.试求反应过程的Q、W、ΔrU、ΔrS和ΔrG。
 答案
答案
 更多“已知某反应:A(g)+B(s)=C(g)+D(s)的ΔrH=-80.25kJ。反应在300K,100kPa下发生,体系做了最大功”相关的问题
更多“已知某反应:A(g)+B(s)=C(g)+D(s)的ΔrH=-80.25kJ。反应在300K,100kPa下发生,体系做了最大功”相关的问题
第1题
已知反应NiO(s)+CO(g)=Ni(s)+CO2(g)的
Kθ(936K)=4.54×102.Kθ(1027K)=2.55×103.若在上述温度范围内△Cp=0p(1)试求此反应在1000K时的△rGmθ、△rHmθ原和△rAmθ;(2)若产物中的镍与某金属生成固溶体(合金),当反应在1000K达到平衡
时,p(CO2)/p(CO)-1.05×103求固溶体中镍的活度,并指出所选的标准态.
第2题
A.K1+K2
B.K1-K2
C.K1?K2
D.K1/K2
第3题

第4题
A.-75.9
B.75.9
C.-145.3
D.145.3
第5题
第6题
已知反应2A(g)+2B(s)=2C(g)+D(g)的△rH<O,要提高A(g)的转化率理论上可以采取的方法是()。
A.高温低压
B.低温低压
C.低温高压
D.高温高压
第7题
已知下列热化学方程式: Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g);qp=-27.6 kJmol-1 3Fe2O3(s)+C0(g)=2Fe3O4(s)+CO2(g);qp=-58.6 kJmol-1 Fe3O4(s)+C0(g)=3FeO(s)+CO2(g);qp=38.1 kJmol-1 不用查表,试计算下列反应的g。。 FeO(S)+CO(g)=Fe(S)+CO2(g)
第8题
已知在18℃,0.1MPa下反应H2(g)+I2(g)→2HI(g)的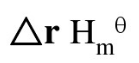 =-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2(1)在沸点184.3℃,0.1MPa下蒸发时吸热42.7kJ·mol-1。在18~113℃区间Cp,m(I2,s)=55.6J·K-1·mol-1,在13.5~184.3℃区间Cp,m(12,1)=62.8J·K-1·mol-1,在184.3~200℃区间Cp,m(I2,g)=(35.56-5.4×10-3T/K)J·K-1·mol-1,在18~200℃区间Cp,m(H2,g)=(29.08-0.84×10-3T/K)J·K-1·mol-1,Cp,m(HI,g)=(28.07-2.1×10-3T/K)J·K-1·mol-1。求在200℃时,反应H2(g)+I2(g)===2HI(g)的
=-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2(1)在沸点184.3℃,0.1MPa下蒸发时吸热42.7kJ·mol-1。在18~113℃区间Cp,m(I2,s)=55.6J·K-1·mol-1,在13.5~184.3℃区间Cp,m(12,1)=62.8J·K-1·mol-1,在184.3~200℃区间Cp,m(I2,g)=(35.56-5.4×10-3T/K)J·K-1·mol-1,在18~200℃区间Cp,m(H2,g)=(29.08-0.84×10-3T/K)J·K-1·mol-1,Cp,m(HI,g)=(28.07-2.1×10-3T/K)J·K-1·mol-1。求在200℃时,反应H2(g)+I2(g)===2HI(g)的 。
。
第9题
已知下列100kPa,298K时的热力学数据:
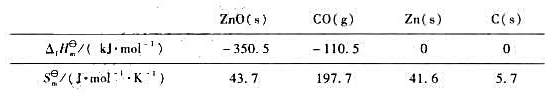
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
第10题
气相反应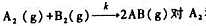 和B2均为一级.现在一个含有过量固体A2(s)
和B2均为一级.现在一个含有过量固体A2(s)
的反应器中充人50.663kPa的B2(g).已知673.2K时以反应的速率常数k=9.869x10-9kPa-1.
g-1,A,(s)的饱和蒸气压为121.59kPa[假设,A2(s)与A2(g)处于快速平衡],且没有逆反应.
(1)计算所加入的B2(g)反应掉一半所需要的时间;
(2)验证下述机理符合二级反应速率方程.
