 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算在pH=2.0,C2O42-总浓度为0.010mol/L的溶液中CaC2O4的溶解度。
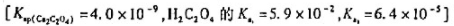
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
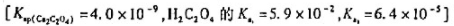
 答案
答案
 更多“计算在pH=2.0,C2O42-总浓度为0.010mol/L的溶液中CaC2O4的溶解度。”相关的问题
更多“计算在pH=2.0,C2O42-总浓度为0.010mol/L的溶液中CaC2O4的溶解度。”相关的问题
第1题
A.[H2C2O4]+[HC2O4-]+[C2O42-] B.[HC2O4-]+[C2O42-]
C.[HC2O4-] D.[C2O42-]
第2题
第4题
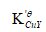 ,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
第6题
已知M(NH3)42+的 为2.0、5.0、7.0、10.0; M(OH)42+的
为2.0、5.0、7.0、10.0; M(OH)42+的 为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?
为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?
第7题
Q美=50-5P美
Q日=16-P日
式中,Q美,P美,Q日,P日分别为两国市场的销售量(单位:万个)和价格(单位:美元)。
(1)假定生产这种磁盘的边际成本是常数。为2美元。问该公司在这两个市场上的最优价格和最优销售量分别是多少?
(2)如这种磁盘的平均变动成本为2.0美元,年总固定成本为20万元,问该公司实行差别定价的总利润是多少?
第8题